Lista de elementos
»
actínio
»
alumínio
»
amerício
»
argão
»
arsênico
»
astatine
»
azoto
»
bário
»
Berílio
»
bismuto
»
bohrium
»
Boro
»
bromo
»
cádmio
»
cálcio
»
carbono
»
cério
»
césio
»
cloro
»
cobalto
»
cobre
»
crômio
»
dubnium
»
enxofre
»
erbium
»
escândio
»
estanho
»
európio
»
fermium
»
ferro
»
fleróvio
»
flúor
»
fósforo
»
francium
»
gálio
»
germânio
»
háfnio
»
hassium
»
hélio
»
holmium
»
índio
»
iodo
»
irídio
»
itérbio
»
ítrio
»
lantânio
»
lead
»
lítio
»
lutécio
»
magnésio
»
manganês
»
mercúrio
»
neodímio
»
néon
»
neptúnio
»
Nihonium
»
nióbio
»
níquel
»
nobelium
»
ósmio
»
ouro
»
oxigênio
»
paládio
»
platina
»
plutônio
»
polônio
»
potássio
»
Prata
»
promécio
»
radão
»
rádio
»
rênio
»
ródio
»
rubídio
»
rutênio
»
samário
»
selênio
»
silício
»
sódio
»
tálio
»
tântalo
»
tecnécio
»
telúrio
»
Tennesse
»
térbio
»
titânio
»
tório
»
túlio
»
urânio
»
vanádio
»
xênon
»
zinco
»
zircônio
C - carbono - OUTRO NÃO METÁLICO
O carbono é um elemento químico essencial à vida e à fabricação de produtos de todos os tipos. É representado pelo símbolo C e é encontrado em abundância no meio ambiente como carbono orgânico (como no carvão, hidrocarbonetos, etc.) e na forma inorgânica (como dióxido de carbono [CO2], monóxido de carbono carbono [CO], etc.). É um elemento vital da vida organizada na Terra.
O carbono é incolor, inodoro e se combina com outros elementos para formar compostos orgânicos e inorgânicos. É considerado um dos três elementos que desempenham um papel importante na química orgânica (junto com o hidrogênio e o oxigênio). O carbono se liga a si mesmo e a outros elementos para formar moléculas cujas propriedades são determinadas pelo tipo de ligação entre os átomos de carbono.
O carbono é um elemento versátil e as moléculas que ele forma podem ter propriedades variadas. As propriedades mais importantes do carbono são a condutividade elétrica, a resistência térmica e a capacidade de absorver umidade. Os produtos feitos de carbono são amplamente utilizados na indústria e na vida cotidiana. Os principais produtos à base de carbono são combustíveis, plásticos, corantes, tintas, aço, têxteis e produtos químicos para cosméticos e medicamentos.
O carbono também é um elemento importante para a produção e armazenamento de energia. O carbono é usado para gerar energia em usinas de energia e pode ser armazenado na forma de carvão, gás natural e petróleo. Os combustíveis fósseis podem ser convertidos em energia a partir do carbono que contêm. O carbono também pode ser armazenado na forma de biomassa (planta orgânica ou matéria animal), dióxido de carbono ou produtos químicos à base de carbono.
O carbono é incolor, inodoro e se combina com outros elementos para formar compostos orgânicos e inorgânicos. É considerado um dos três elementos que desempenham um papel importante na química orgânica (junto com o hidrogênio e o oxigênio). O carbono se liga a si mesmo e a outros elementos para formar moléculas cujas propriedades são determinadas pelo tipo de ligação entre os átomos de carbono.
O carbono é um elemento versátil e as moléculas que ele forma podem ter propriedades variadas. As propriedades mais importantes do carbono são a condutividade elétrica, a resistência térmica e a capacidade de absorver umidade. Os produtos feitos de carbono são amplamente utilizados na indústria e na vida cotidiana. Os principais produtos à base de carbono são combustíveis, plásticos, corantes, tintas, aço, têxteis e produtos químicos para cosméticos e medicamentos.
O carbono também é um elemento importante para a produção e armazenamento de energia. O carbono é usado para gerar energia em usinas de energia e pode ser armazenado na forma de carvão, gás natural e petróleo. Os combustíveis fósseis podem ser convertidos em energia a partir do carbono que contêm. O carbono também pode ser armazenado na forma de biomassa (planta orgânica ou matéria animal), dióxido de carbono ou produtos químicos à base de carbono.
Sintético
Radioativo
Líquido
Gasoso
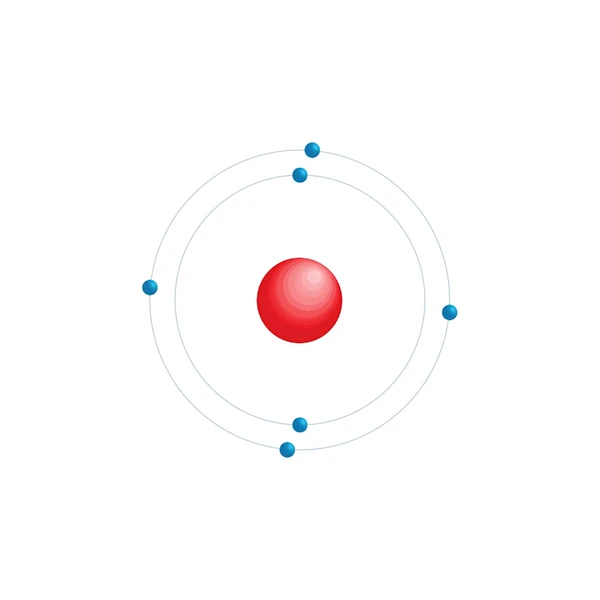
Diagrama de configuração eletrônica
| Nome | carbono |
| Número | 6 |
| Atômico | 12.0112 |
| Símbolo | C |
| Fusão | 3550 |
| Ebulição | 4827 |
| Densidade | 2.267 |
| Período | 2 |
| Grupo | 14 |
| Descoberta | 0 Prehistoric |
| Abundância | 200 |
| Raio | 0.91 |
| Eletronegatividade | 2.55 |
| Ionização | 11.2603 |
| Número de isótopos | 7 |
| Configuração eletrônica | [He] 2s2 2p2 |
| Estados de oxidação | -4,-3,-2,-1,1,2,3,4 |
| Elétron por nível de energia | 2,4 |
| Mineral | Dureza | Densidade |
| Abelsonite | 2.00 / 2.50 | 1.45 |
| Abenakiite-(Ce) | 4.00 / 4.00 | 3.21 |
| Acetamide | 1.00 / 1.50 | 1.17 |
| Adamsite-(Y) | 3.00 / 3.00 | |
| Aerinite | 3.00 / 3.00 | 2.48 |
| Afghanite | 5.50 / 6.00 | 2.55 |
| Agaite | 6.99 | |
| Agricolaite | 4.00 / 4.00 | 3.53 |
| Albrechtschraufite | 2.00 / 3.00 | 2.60 |
| Alexkhomyakovite | ||
| Alloriite | 5.00 / 5.00 | 2.35 |
| Alstonite | 4.00 / 4.50 | 3.69 |
| Alumohydrocalcite | 2.50 / 2.50 | 2.23 |
| Âmbar | 2.00 / 2.50 | 1.10 |
| Amonite | 6.00 / 7.00 | 3.20 |
| Ancylite-(Ce) | 4.50 / 4.50 | 3.90 |
| Ancylite-(La) | 4.00 / 4.50 | 3.88 |
| Andersonite | 2.50 / 2.50 | 2.79 |
| Ankerite | 3.50 / 4.00 | 3.00 |
| Antipinite | 2.00 / 2.00 | 2.55 |
| Aragonite | 3.50 / 4.00 | 2.93 |
| Arisite-(Ce) | ||
| Arisite-(La) | 3.00 / 3.50 | 4.07 |
| Armangite | 4.00 / 4.00 | 4.43 |
| Artinite | 2.50 / 2.50 | 2.00 |
| Ashburtonite | 4.69 | |
| Ashcroftine-(Y) | 5.00 / 5.00 | 2.61 |
| Astrocyanite-(Ce) | 2.00 / 3.00 | 3.80 |
| Aurichalcite | 2.00 / 2.00 | 3.64 |
| Azurita | 3.50 / 4.00 | 3.77 |
| Balliranoite | ||
| Barbertonite | 1.50 / 2.00 | 2.10 |
| Barentsite | 3.00 / 3.00 | 2.56 |
| Barringtonite | 2.83 | |
| Barstowite | 3.00 / 3.00 | 5.50 |
| Barytocalcite | 4.00 / 4.00 | 3.64 |
| Bastnäsite-(Ce) | 4.00 / 5.00 | 4.95 |
| Bastnäsite-(La) | 4.00 / 5.00 | 4.95 |
| Bastnäsite-(Nd) | 4.00 / 4.50 | 5.23 |
| Bastnäsite-(Y) | 4.00 / 4.50 | 4.90 |
| Bayleyite | 2.05 | |
| Baylissite | 2.00 | |
| Benstonite | 3.00 / 4.00 | 3.60 |
| Beyerite | 2.00 / 3.00 | 6.56 |
| Bijvoetite-(Y) | 2.00 / 2.00 | 3.90 |
| Biraite-(Ce) | 5.00 / 5.00 | 4.76 |
| Birunite | 2.00 / 2.00 | 2.36 |
| Bismutite | 4.00 / 4.00 | 7.00 |
| Blatonite | 2.00 / 3.00 | 3.99 |
| Bonshtedtite | 4.00 / 4.00 | 2.95 |
| Borcarite | 4.00 / 4.00 | 2.77 |
| Bosoite | ||
| Bradleyite | 3.00 / 4.00 | 2.73 |
| Braunerite | ||
| Brenkite | 3.10 | |
| Brianyoungite | 2.00 / 2.50 | 3.93 |
| Britvinite | 3.00 / 3.00 | 5.51 |
| Brugnatellite | 2.00 / 2.00 | 2.14 |
| Burbankite | 3.50 / 3.50 | 3.50 |
| Burkeite | 3.50 / 3.50 | 2.57 |
| Bussenite | 4.00 / 4.00 | 3.63 |
| Bütschliite | 2.00 | |
| Calcioancylite-(Ce) | 4.00 / 4.50 | |
| Calcioancylite-(Nd) | 4.00 / 4.50 | |
| Calcioburbankite | 3.00 / 4.00 | 3.45 |
| Calcita | 3.00 / 3.00 | 2.71 |
| Calclacite | 1.00 | |
| Caledonite | 2.50 / 3.00 | 5.70 |
| Calkinsite-(Ce) | 2.50 / 2.50 | 3.27 |
| Callaghanite | 3.00 / 3.50 | 2.71 |
| Camérolaite | 3.10 | |
| Canavesite | 1.80 | |
| Cancrinite | 6.00 / 6.00 | 2.40 |
| Cancrisilite | 5.00 / 5.00 | 2.40 |
| Caoxite | 2.00 / 2.50 | 1.85 |
| Carboborite | 2.00 / 2.00 | 2.12 |
| Carbobystrite | 6.00 / 6.00 | 2.37 |
| Carbocernaite | 3.00 / 3.00 | 3.53 |
| Carbokentbrooksite | 5.00 / 5.00 | 3.14 |
| Carbonate-fluorapatite | 5.00 / 5.00 | 3.12 |
| Carbonate-hydroxylapatite | 5.00 / 5.00 | 3.00 |
| Carbonatecyanotrichite | 2.00 / 2.00 | 2.65 |
| Carborandita | ||
| Caresite | 2.00 / 2.00 | 2.57 |
| Carletonite | 4.00 / 4.50 | 2.45 |
| Carpathite | 1.50 / 1.50 | 1.29 |
| Carraraite | ||
| Carrboydite | 2.50 | |
| Caysichite-(Y) | 4.50 / 4.50 | 3.03 |
| Cebaite-(Ce) | 4.50 / 5.00 | 4.81 |
| Cebaite-(Nd) | 4.50 / 5.00 | 4.80 |
| Cejkaite | 3.67 | |
| Cerusite | 3.00 / 3.50 | 6.50 |
| Chalconatronite | 1.00 / 2.00 | 2.27 |
| Chanabayaite | 2.00 / 2.00 | 1.46 |
| Chaoite | 1.00 / 2.00 | 3.33 |
| Charmarite | ||
| Chibaite | 6.50 / 7.00 | 1.93 |
| Chlorartinite | 1.87 |
 mineraly.fr
mineraly.fr
 mineraly.co.uk
mineraly.co.uk
 mineraly.com.de
mineraly.com.de
 mineraly.it
mineraly.it
 mineraly.es
mineraly.es
 mineraly.nl
mineraly.nl
 mineraly.pt
mineraly.pt
 mineraly.se
mineraly.se