Lista de elementos
»
actínio
»
alumínio
»
amerício
»
argão
»
arsênico
»
astatine
»
azoto
»
bário
»
Berílio
»
bismuto
»
bohrium
»
Boro
»
bromo
»
cádmio
»
cálcio
»
carbono
»
cério
»
césio
»
cloro
»
cobalto
»
cobre
»
crômio
»
dubnium
»
enxofre
»
erbium
»
escândio
»
estanho
»
európio
»
fermium
»
ferro
»
fleróvio
»
flúor
»
fósforo
»
francium
»
gálio
»
germânio
»
háfnio
»
hassium
»
hélio
»
holmium
»
índio
»
iodo
»
irídio
»
itérbio
»
ítrio
»
lantânio
»
lead
»
lítio
»
lutécio
»
magnésio
»
manganês
»
mercúrio
»
neodímio
»
néon
»
neptúnio
»
Nihonium
»
nióbio
»
níquel
»
nobelium
»
ósmio
»
ouro
»
oxigênio
»
paládio
»
platina
»
plutônio
»
polônio
»
potássio
»
Prata
»
promécio
»
radão
»
rádio
»
rênio
»
ródio
»
rubídio
»
rutênio
»
samário
»
selênio
»
silício
»
sódio
»
tálio
»
tântalo
»
tecnécio
»
telúrio
»
Tennesse
»
térbio
»
titânio
»
tório
»
túlio
»
urânio
»
vanádio
»
xênon
»
zinco
»
zircônio
Xe - xênon - NENHUM METAL GASOSO NOBRE
Xenon é um elemento químico natural, número atômico 54, símbolo Xe e massa atômica 131.293. É um gás nobre inodoro e incolor que é encontrado na atmosfera da Terra em concentrações muito baixas. É quimicamente inerte e estável em seu estado normal.
O xenônio tem uma massa molar de 131,3 g/mol e uma pressão de vapor de 16,6 kPa a 25°C. É mais pesado que o ar e à pressão atmosférica seu ponto de ebulição é -111,8°C. Tem um ponto de fusão de -108,1°C e uma densidade relativamente baixa de 4,94 g/l a 25°C.
O xenônio é amplamente utilizado por suas propriedades de resfriamento e luminosidade. É usado para produzir luzes fluorescentes e para aplicações médicas, como scanners de raios-x ou lasers de xenônio. Também é usado para encher pneus, produzir feixes de plasma e fazer bombas de vácuo. O xenônio também é usado na indústria automotiva para faróis e para encher tanques de combustível de veículos novos. Além disso, o xenônio é usado em pesquisas científicas para estudar vários efeitos físicos e químicos, como difusão de gás e absorção de radiação.
O xenônio tem uma massa molar de 131,3 g/mol e uma pressão de vapor de 16,6 kPa a 25°C. É mais pesado que o ar e à pressão atmosférica seu ponto de ebulição é -111,8°C. Tem um ponto de fusão de -108,1°C e uma densidade relativamente baixa de 4,94 g/l a 25°C.
O xenônio é amplamente utilizado por suas propriedades de resfriamento e luminosidade. É usado para produzir luzes fluorescentes e para aplicações médicas, como scanners de raios-x ou lasers de xenônio. Também é usado para encher pneus, produzir feixes de plasma e fazer bombas de vácuo. O xenônio também é usado na indústria automotiva para faróis e para encher tanques de combustível de veículos novos. Além disso, o xenônio é usado em pesquisas científicas para estudar vários efeitos físicos e químicos, como difusão de gás e absorção de radiação.
Sintético
Radioativo
Líquido
Gasoso
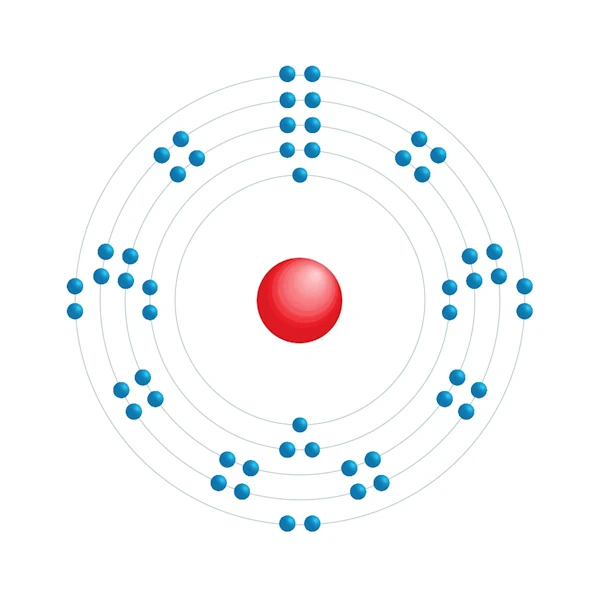
Diagrama de configuração eletrônica
| Nome | xênon |
| Número | 54 |
| Atômico | 131.293 |
| Símbolo | Xe |
| Fusão | -111.9 |
| Ebulição | -107 |
| Densidade | 0.005887 |
| Período | 5 |
| Grupo | 18 |
| Descoberta | 1898 Ramsay and Travers |
| Abundância | 0.001 |
| Raio | 1.2 |
| Eletronegatividade | 0 |
| Ionização | 12.1298 |
| Número de isótopos | 31 |
| Configuração eletrônica | [Kr] 4d10 5s2 5p6 |
| Estados de oxidação | 2,4,6,8 |
| Elétron por nível de energia | 2,8,18,18,8 |
 mineraly.fr
mineraly.fr
 mineraly.co.uk
mineraly.co.uk
 mineraly.com.de
mineraly.com.de
 mineraly.it
mineraly.it
 mineraly.es
mineraly.es
 mineraly.nl
mineraly.nl
 mineraly.pt
mineraly.pt
 mineraly.se
mineraly.se