Lista de elementos
»
actínio
»
alumínio
»
amerício
»
argão
»
arsênico
»
astatine
»
azoto
»
bário
»
Berílio
»
bismuto
»
bohrium
»
Boro
»
bromo
»
cádmio
»
cálcio
»
carbono
»
cério
»
césio
»
cloro
»
cobalto
»
cobre
»
crômio
»
dubnium
»
enxofre
»
erbium
»
escândio
»
estanho
»
európio
»
fermium
»
ferro
»
fleróvio
»
flúor
»
fósforo
»
francium
»
gálio
»
germânio
»
háfnio
»
hassium
»
hélio
»
holmium
»
índio
»
iodo
»
irídio
»
itérbio
»
ítrio
»
lantânio
»
lead
»
lítio
»
lutécio
»
magnésio
»
manganês
»
mercúrio
»
neodímio
»
néon
»
neptúnio
»
Nihonium
»
nióbio
»
níquel
»
nobelium
»
ósmio
»
ouro
»
oxigênio
»
paládio
»
platina
»
plutônio
»
polônio
»
potássio
»
Prata
»
promécio
»
radão
»
rádio
»
rênio
»
ródio
»
rubídio
»
rutênio
»
samário
»
selênio
»
silício
»
sódio
»
tálio
»
tântalo
»
tecnécio
»
telúrio
»
Tennesse
»
térbio
»
titânio
»
tório
»
túlio
»
urânio
»
vanádio
»
xênon
»
zinco
»
zircônio
Na - sódio - METAL ALCALINO
O sódio é um elemento químico da família dos metais alcalinos que possui o símbolo químico Na. É o elemento fundamental mais abundante nos oceanos e é um dos elementos mais abundantes na Terra.
O sódio puro é um metal macio, branco prateado. Foi descoberto por Sir Humphrey Davy em 1807. É muito reativo e reage muito facilmente com água para formar hidrogênio e hidróxido de sódio.
O sódio é amplamente utilizado na indústria alimentícia, sendo utilizado para salgar alimentos. Também é amplamente utilizado na indústria química e para fazer produtos de sal. O sódio também é usado na indústria de alumínio para produzir alumínio.
As principais características do sódio são sua baixa densidade e sua baixa condutividade térmica e elétrica. Isso significa que é um excelente isolante térmico e elétrico. Ele também tem uma baixa pressão de vapor e é muito solúvel em água.
As propriedades químicas do sódio devem-se principalmente à sua alta reatividade. O sódio é muito reativo com água, oxigênio, ácido sulfúrico e outras substâncias. Os produtos da reação com oxigênio são óxidos, enquanto aqueles com água são hidróxidos e carbonatos.
O sódio é usado em muitas aplicações industriais porque é muito reativo e abundante. Alguns dos usos comuns incluem fazer sais e usar como catalisador em certas reações químicas. Também é usado na indústria alimentícia para conservar os alimentos e melhorar seu sabor. Também é usado para a produção de alumínio e para o tratamento de águas residuais.
O sódio puro é um metal macio, branco prateado. Foi descoberto por Sir Humphrey Davy em 1807. É muito reativo e reage muito facilmente com água para formar hidrogênio e hidróxido de sódio.
O sódio é amplamente utilizado na indústria alimentícia, sendo utilizado para salgar alimentos. Também é amplamente utilizado na indústria química e para fazer produtos de sal. O sódio também é usado na indústria de alumínio para produzir alumínio.
As principais características do sódio são sua baixa densidade e sua baixa condutividade térmica e elétrica. Isso significa que é um excelente isolante térmico e elétrico. Ele também tem uma baixa pressão de vapor e é muito solúvel em água.
As propriedades químicas do sódio devem-se principalmente à sua alta reatividade. O sódio é muito reativo com água, oxigênio, ácido sulfúrico e outras substâncias. Os produtos da reação com oxigênio são óxidos, enquanto aqueles com água são hidróxidos e carbonatos.
O sódio é usado em muitas aplicações industriais porque é muito reativo e abundante. Alguns dos usos comuns incluem fazer sais e usar como catalisador em certas reações químicas. Também é usado na indústria alimentícia para conservar os alimentos e melhorar seu sabor. Também é usado para a produção de alumínio e para o tratamento de águas residuais.
Sintético
Radioativo
Líquido
Gasoso
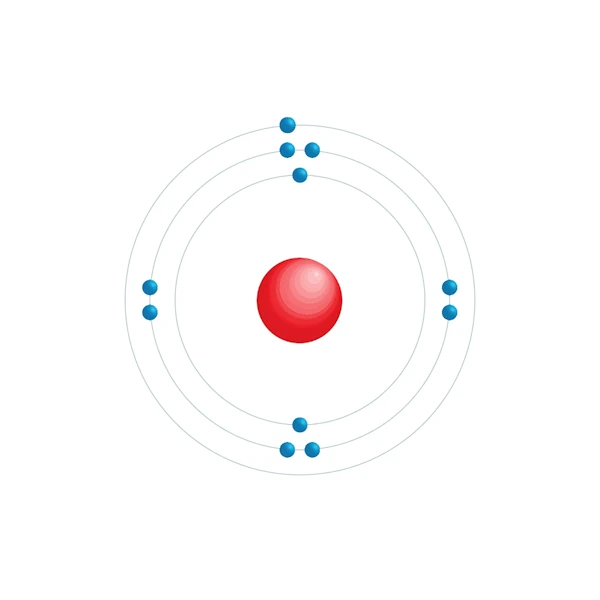
Diagrama de configuração eletrônica
| Nome | sódio |
| Número | 11 |
| Atômico | 22.98976928 |
| Símbolo | Na |
| Fusão | 97.8 |
| Ebulição | 892 |
| Densidade | 0.971 |
| Período | 3 |
| Grupo | 1 |
| Descoberta | 1807 Davy |
| Abundância | 23600 |
| Raio | 2.2 |
| Eletronegatividade | 0.93 |
| Ionização | 5.1391 |
| Número de isótopos | 7 |
| Configuração eletrônica | [Ne] 3s1 |
| Estados de oxidação | -1,1 |
| Elétron por nível de energia | 2,8,1 |
| Mineral | Dureza | Densidade |
| Abenakiite-(Ce) | 4.00 / 4.00 | 3.21 |
| Acmonidesite | ||
| Actinolite | 5.50 / 5.50 | 2.98 |
| Adamsite-(Y) | 3.00 / 3.00 | |
| Adranosite | ||
| Adranosite-(Fe) | 2.20 | |
| Aegirine | 6.00 / 6.50 | 3.50 |
| Aegirine-augite | 6.00 / 6.00 | 3.40 |
| Aenigmatite | 5.00 / 6.00 | 3.74 |
| Aerinite | 3.00 / 3.00 | 2.48 |
| Afghanite | 5.50 / 6.00 | 2.55 |
| Agrellite | 5.50 / 5.50 | 2.88 |
| Aiolosite | 3.59 | |
| Ajoite | 2.96 | |
| Albite | 7.00 / 7.00 | 2.61 |
| Alexkhomyakovite | ||
| Alflarsenite | 4.00 / 4.00 | 2.61 |
| Aliettite | 1.00 / 2.00 | |
| Alloriite | 5.00 / 5.00 | 2.35 |
| Alluaivite | 5.00 / 6.00 | 2.76 |
| Alluaudite | 5.00 / 5.50 | 3.45 |
| Almarudite | 6.00 / 6.00 | 2.71 |
| Alnaperbøeite-(Ce) | ||
| Alsakharovite-Zn | 5.00 / 5.00 | 2.90 |
| Altisite | 6.00 / 6.00 | 2.64 |
| Alum-(Na) | 3.00 / 3.00 | 1.67 |
| Alumino-ferrobarroisite | ||
| Alumino-ferrowinchite | ||
| Alumino-magnesiotaramite | ||
| Alumino-ottoliniite | ||
| Aluminobarroisite | 5.00 / 6.00 | 2.94 |
| Aluminokatophorite | 5.00 / 6.00 | |
| Aluminowinchite | ||
| Alumoåkermanite | 4.00 / 5.00 | 3.00 |
| Amarillite | 2.50 / 3.00 | 2.19 |
| Amblygonite | 5.50 / 6.00 | 2.98 |
| Ameghinite | 2.00 / 3.00 | 2.02 |
| Amicite | 5.00 / 5.50 | 2.06 |
| Analcime | 5.00 / 5.00 | 2.30 |
| Andersonite | 2.50 / 2.50 | 2.79 |
| Andesine | 7.00 / 7.00 | 2.66 |
| Andrianovite | 5.00 / 5.00 | 3.02 |
| Angarfite | 2.50 / 2.50 | 2.77 |
| Anorthite | 6.00 / 6.00 | 2.72 |
| Anorthoclase | 6.00 / 6.00 | 2.57 |
| Antipinite | 2.00 / 2.00 | 2.55 |
| Apexite | 2.00 / 2.00 | 1.74 |
| Aphthitalite | 3.00 / 3.00 | 2.70 |
| Aqualite | 4.00 / 5.00 | 2.66 |
| Arapovite | 5.50 / 6.00 | 3.43 |
| Arctite | 5.00 / 5.00 | 3.11 |
| Ardennite-(V) | 6.00 / 7.00 | 3.55 |
| Arfvedsonite | 5.50 / 6.00 | 3.44 |
| Arisite-(Ce) | ||
| Arisite-(La) | 3.00 / 3.50 | 4.07 |
| Aristarainite | 3.50 / 3.50 | 2.03 |
| Armbrusterite | 3.50 / 3.50 | 2.78 |
| Arnhemite | 2.33 | |
| Arrojadite-(BaFe) | 3.54 | |
| Arrojadite-(BaNa) | ||
| Arrojadite-(KFe) | 5.00 / 5.00 | 3.50 |
| Arrojadite-(KNa) | ||
| Arrojadite-(NaFe) | ||
| Arrojadite-(PbFe) | 4.00 / 5.00 | |
| Arrojadite-(SrFe) | ||
| Arseniopleite | 3.50 / 3.50 | 4.22 |
| Arsmirandite | ||
| Ashcroftine-(Y) | 5.00 / 5.00 | 2.61 |
| Aspidolite | 2.00 / 3.00 | 2.89 |
| Astrophyllite | 3.00 / 3.50 | 3.30 |
| Augite | 5.00 / 6.50 | 3.20 |
| Bakhchisaraitsevite | 2.00 / 2.50 | 2.50 |
| Balliranoite | ||
| Banalsite | 6.00 / 6.00 | 3.07 |
| Bannermanite | 3.50 | |
| Bannisterite | 4.00 / 4.00 | 2.83 |
| Barahonaite-(Al) | ||
| Barahonaite-(Fe) | 3.03 | |
| Barentsite | 3.00 / 3.00 | 2.56 |
| Bario-olgite | 4.00 / 4.50 | 4.00 |
| Barnesite | 3.00 / 3.00 | 3.15 |
| Barrerite | 3.00 / 4.00 | 2.13 |
| Barroisite | 5.00 / 6.00 | 3.00 |
| Barrydawsonite-(Y) | ||
| Barytolamprophyllite | 2.00 / 3.00 | 3.62 |
| Batiferrite | 6.00 / 6.00 | |
| Batisite | 5.90 / 5.90 | 3.43 |
| Bazzite | 6.50 / 6.50 | 2.80 |
| Bederite | 5.00 / 5.00 | 3.48 |
| Beidellite | 1.00 / 2.00 | 2.00 |
| Belakovskiite | ||
| Bellbergite | 5.00 / 5.00 | 2.20 |
| Belovite-(Ce) | 5.00 / 5.00 | 4.19 |
| Belovite-(La) | 5.00 / 5.00 | 4.19 |
| Benyacarite | 2.50 / 3.00 | 2.40 |
| Beryllonite | 5.50 / 6.00 | 2.80 |
| Berzeliite | 4.50 / 5.00 | 4.08 |
| Betalomonosovite | ||
| Betpakdalite-NaCa | 2.89 |
 mineraly.fr
mineraly.fr
 mineraly.co.uk
mineraly.co.uk
 mineraly.com.de
mineraly.com.de
 mineraly.it
mineraly.it
 mineraly.es
mineraly.es
 mineraly.nl
mineraly.nl
 mineraly.pt
mineraly.pt
 mineraly.se
mineraly.se