Lista de elementos
»
actínio
»
alumínio
»
amerício
»
argão
»
arsênico
»
astatine
»
azoto
»
bário
»
Berílio
»
bismuto
»
bohrium
»
Boro
»
bromo
»
cádmio
»
cálcio
»
carbono
»
cério
»
césio
»
cloro
»
cobalto
»
cobre
»
crômio
»
dubnium
»
enxofre
»
erbium
»
escândio
»
estanho
»
európio
»
fermium
»
ferro
»
fleróvio
»
flúor
»
fósforo
»
francium
»
gálio
»
germânio
»
háfnio
»
hassium
»
hélio
»
holmium
»
índio
»
iodo
»
irídio
»
itérbio
»
ítrio
»
lantânio
»
lead
»
lítio
»
lutécio
»
magnésio
»
manganês
»
mercúrio
»
neodímio
»
néon
»
neptúnio
»
Nihonium
»
nióbio
»
níquel
»
nobelium
»
ósmio
»
ouro
»
oxigênio
»
paládio
»
platina
»
plutônio
»
polônio
»
potássio
»
Prata
»
promécio
»
radão
»
rádio
»
rênio
»
ródio
»
rubídio
»
rutênio
»
samário
»
selênio
»
silício
»
sódio
»
tálio
»
tântalo
»
tecnécio
»
telúrio
»
Tennesse
»
térbio
»
titânio
»
tório
»
túlio
»
urânio
»
vanádio
»
xênon
»
zinco
»
zircônio
mineralogia
elementos
O oxigênio
O - oxigênio - OUTRO NÃO METÁLICO
O oxigênio (símbolo químico O) é um elemento químico da família dos calcogênios, subgrupo 16 da tabela periódica dos elementos. É o maior componente da atmosfera terrestre, representando cerca de 20,9% do volume total.
O oxigênio é um composto muito reativo e, portanto, muito importante para muitas reações químicas. É o terceiro elemento mais abundante no universo depois do hidrogênio e do hélio. É capaz de formar ligações covalentes com outros átomos e pode se combinar com eles para formar moléculas mais complexas, como compostos orgânicos. O oxigênio é um gás em seu estado normal, é um gás incolor, inodoro e insípido. Sua fórmula química é O2 e sua massa molar é 32 g/mol.
O oxigênio é um gás muito reativo, pois possui oito elétrons em sua camada externa de elétrons. É um oxidante forte e é muito útil em várias reações químicas. Também é muito solúvel em água e é a principal fonte de oxigênio disponível para os seres vivos. O oxigênio também é combustível e é muito utilizado em indústrias e laboratórios por suas propriedades oxidantes.
O oxigênio é o principal componente dos combustíveis fósseis e, portanto, muito importante no processo de combustão. É amplamente utilizado para várias aplicações industriais, incluindo a fabricação de metais, produtos químicos, fertilizantes, medicamentos e produtos farmacêuticos. Além dos usos industriais, o oxigênio é usado no tratamento médico para ajudar pessoas com doenças respiratórias graves. Também é usado por muitas indústrias, como aeronáutica, astronáutica e esportes radicais.
O oxigênio é um composto muito reativo e, portanto, muito importante para muitas reações químicas. É o terceiro elemento mais abundante no universo depois do hidrogênio e do hélio. É capaz de formar ligações covalentes com outros átomos e pode se combinar com eles para formar moléculas mais complexas, como compostos orgânicos. O oxigênio é um gás em seu estado normal, é um gás incolor, inodoro e insípido. Sua fórmula química é O2 e sua massa molar é 32 g/mol.
O oxigênio é um gás muito reativo, pois possui oito elétrons em sua camada externa de elétrons. É um oxidante forte e é muito útil em várias reações químicas. Também é muito solúvel em água e é a principal fonte de oxigênio disponível para os seres vivos. O oxigênio também é combustível e é muito utilizado em indústrias e laboratórios por suas propriedades oxidantes.
O oxigênio é o principal componente dos combustíveis fósseis e, portanto, muito importante no processo de combustão. É amplamente utilizado para várias aplicações industriais, incluindo a fabricação de metais, produtos químicos, fertilizantes, medicamentos e produtos farmacêuticos. Além dos usos industriais, o oxigênio é usado no tratamento médico para ajudar pessoas com doenças respiratórias graves. Também é usado por muitas indústrias, como aeronáutica, astronáutica e esportes radicais.
Sintético
Radioativo
Líquido
Gasoso
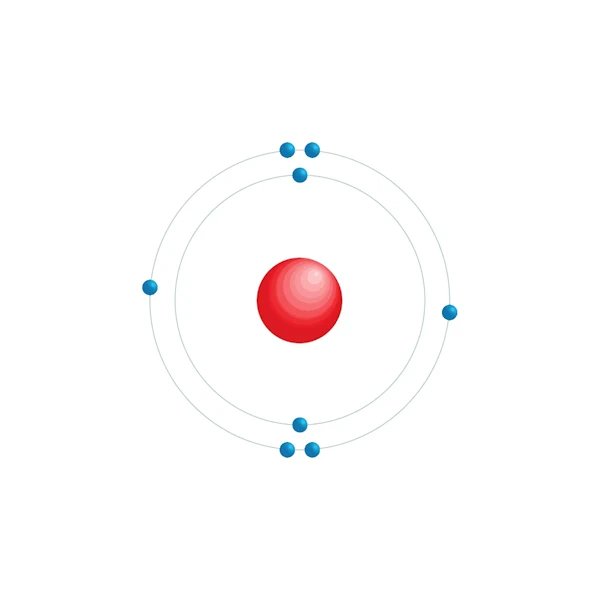
Diagrama de configuração eletrônica
| Nome | oxigênio |
| Número | 8 |
| Atômico | 15.9992 |
| Símbolo | O |
| Fusão | -218.4 |
| Ebulição | -182.9 |
| Densidade | 0.001429 |
| Período | 2 |
| Grupo | 16 |
| Descoberta | 1774 Priestley/Scheele |
| Abundância | 461000 |
| Raio | 0.65 |
| Eletronegatividade | 3.44 |
| Ionização | 13.6181 |
| Número de isótopos | 8 |
| Configuração eletrônica | [He] 2s2 2p4 |
| Estados de oxidação | -2,-1,1,2 |
| Elétron por nível de energia | 2,6 |
| Mineral | Dureza | Densidade |
| Abelha Jaspe | 6.50 / 7.00 | 2.58 |
| Abenakiite-(Ce) | 4.00 / 4.00 | 3.21 |
| Abernathyite | 2.00 / 3.00 | 3.31 |
| Abhurite | 2.00 / 2.00 | 4.29 |
| Abswurmbachite | 6.50 / 6.50 | 4.96 |
| Abuite | ||
| Acetamide | 1.00 / 1.50 | 1.17 |
| Achalaite | ||
| Acmonidesite | ||
| Actinolite | 5.50 / 5.50 | 2.98 |
| Acuminite | 3.50 / 3.50 | 3.30 |
| Adachiite | ||
| Adamite | 3.50 / 3.50 | 4.30 |
| Adamsite-(Y) | 3.00 / 3.00 | |
| Addibischoffite | ||
| Adelite | 5.00 / 5.00 | 3.73 |
| Admontite | 2.00 / 3.00 | 1.82 |
| Adolfpateraite | 2.00 / 2.00 | 4.24 |
| Adranosite | ||
| Adranosite-(Fe) | 2.20 | |
| Adrianite | ||
| Aegirine | 6.00 / 6.50 | 3.50 |
| Aegirine-augite | 6.00 / 6.00 | 3.40 |
| Aenigmatite | 5.00 / 6.00 | 3.74 |
| Aerinite | 3.00 / 3.00 | 2.48 |
| Aerugite | 4.00 / 4.00 | 5.85 |
| Aeschynite-(Ce) | 5.00 / 6.00 | 5.19 |
| Aeschynite-(Nd) | 5.00 / 6.00 | 4.60 |
| Aeschynite-(Y) | 5.00 / 6.00 | 4.85 |
| Afghanite | 5.50 / 6.00 | 2.55 |
| Afmite | ||
| Afwillite | 3.00 / 3.00 | 2.62 |
| Agaite | 6.99 | |
| Agakhanovite-(Y) | 6.00 / 6.00 | 2.67 |
| Agardite-(Ce) | 3.00 / 3.00 | 3.72 |
| Agardite-(La) | 3.00 / 4.00 | 3.72 |
| Agardite-(Nd) | 3.00 / 4.00 | 3.72 |
| Agardite-(Y) | 3.00 / 4.00 | 3.66 |
| Agata | 6.50 / 7.00 | 2.60 |
| Ágata musgo | 6.00 / 6.50 | 2.60 |
| Aglomerado de calcedônia | 6.50 / 7.00 | 2.60 |
| Agrellite | 5.50 / 5.50 | 2.88 |
| Agricolaite | 4.00 / 4.00 | 3.53 |
| Agrinierite | 5.62 | |
| Água-marinha | 7.50 / 8.00 | 2.70 |
| Aheylite | 5.00 / 6.00 | 2.85 |
| Ahlfeldite | 2.00 / 2.50 | 3.37 |
| Ahrensite | 4.14 | |
| Aiolosite | 3.59 | |
| Ajoite | 2.96 | |
| Akaganeite | 3.00 | |
| Akaogiite | ||
| Akatoreite | 6.00 / 6.00 | 3.48 |
| Akdalaite | 7.00 / 7.00 | 3.68 |
| Akermanite | 5.00 / 6.00 | 2.94 |
| Akhtenskite | 4.00 | |
| Akimotoite | ||
| Aklimaite | ||
| Akrochordite | 3.50 / 3.50 | 3.19 |
| Aksaite | 2.50 / 2.50 | 1.99 |
| Alamosite | 4.50 / 4.50 | 6.49 |
| Alanita | 5.50 / 5.50 | 3.30 |
| Alarsite | 3.00 / 3.00 | 3.32 |
| Albertiniite | 2.46 | |
| Albite | 7.00 / 7.00 | 2.61 |
| Albrechtschraufite | 2.00 / 3.00 | 2.60 |
| Alcaparrosaite | 4.00 / 4.00 | 2.81 |
| Aldermanite | 2.00 / 2.00 | 2.00 |
| Aldridgeite | 3.00 / 3.00 | 3.33 |
| Aleksandrovite | 4.00 / 4.50 | 3.07 |
| Alexkhomyakovite | ||
| Alflarsenite | 4.00 / 4.00 | 2.61 |
| Alforsite | 5.00 / 5.00 | 4.73 |
| Alfredopetrovite | 2.50 / 2.50 | 2.50 |
| Alfredstelznerite | ||
| Aliettite | 1.00 / 2.00 | |
| Allactite | 4.50 / 4.50 | 3.00 |
| Allanite-(La) | 6.00 / 6.00 | 3.93 |
| Allanite-(Nd) | ||
| Allanite-(Y) | 5.50 / 5.50 | 3.30 |
| Allanpringite | 3.00 / 3.00 | 2.54 |
| Alleghanyite | 6.00 / 5.00 | 4.00 |
| Allendeite | 4.84 | |
| Allochalcoselite | 3.00 / 4.00 | 4.65 |
| Allophane | 3.00 / 3.00 | 1.90 |
| Alloriite | 5.00 / 5.00 | 2.35 |
| Alluaivite | 5.00 / 6.00 | 2.76 |
| Alluaudite | 5.00 / 5.50 | 3.45 |
| Almandine | 7.00 / 8.00 | 4.09 |
| Almarudite | 6.00 / 6.00 | 2.71 |
| Almeidaite | ||
| Alnaperbøeite-(Ce) | ||
| Alpersite | 2.50 / 2.50 | |
| Alsakharovite-Zn | 5.00 / 5.00 | 2.90 |
| Alstonite | 4.00 / 4.50 | 3.69 |
| Althausite | 3.50 / 3.50 | 2.97 |
| Althupite | 3.50 / 4.00 | 3.90 |
| Altisite | 6.00 / 6.00 | 2.64 |
| Alum-(K) | 2.00 / 2.00 | 1.76 |
 mineraly.fr
mineraly.fr
 mineraly.co.uk
mineraly.co.uk
 mineraly.com.de
mineraly.com.de
 mineraly.it
mineraly.it
 mineraly.es
mineraly.es
 mineraly.nl
mineraly.nl
 mineraly.pt
mineraly.pt
 mineraly.se
mineraly.se